SGDD(立体構造に指南された医薬品設計)は、 いわゆる「合理的創薬:rational drug design」の主要かつ最強の手法です。それは、創薬の標的のタンパク質に対して、化合物が結合するポケットの立体構造を精密に解析し、そのポケットに最適に結合する化合物を、探索したり設計したりシミュレーションするという方法論です。
いわゆる「合理的創薬:rational drug design」の主要かつ最強の手法です。それは、創薬の標的のタンパク質に対して、化合物が結合するポケットの立体構造を精密に解析し、そのポケットに最適に結合する化合物を、探索したり設計したりシミュレーションするという方法論です。
そのためには、タンパク質の立体構造が必要です。
構造生物学にはどんな方法があるの?
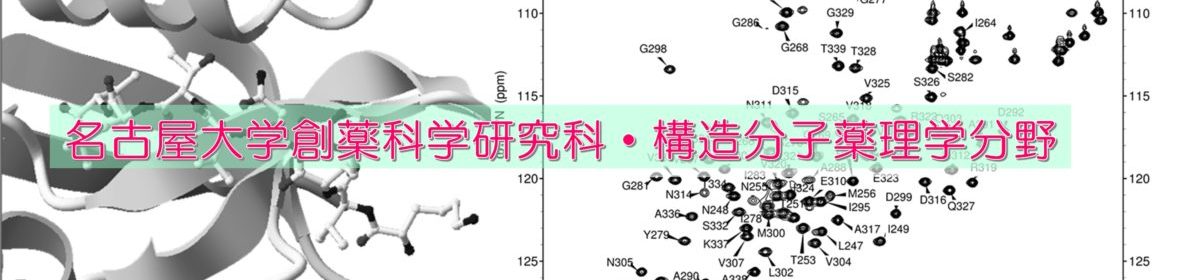
タンパク質・核酸の立体構造を決定するためには、おもにX線結晶解析・NMR・電子顕微鏡の三つの方法論があります。このうち、廣明グループではおもにNMRをメインの手法として、ときにX線結晶解析や電子顕微鏡を組み合わせて用います。X線や電子顕微鏡は私たち単独では不可能ですので、いくつかの共同研究先にお願いして一緒に研究を進めることになります。当研究室のモットーは「適材適所」「持ちつ持たれつ」ですので、ひとつの手法のみにこだわったりすることはあまりありません。
NMR構造生物学には、よい点とわるい点があります。
よい点:「結晶化」しない試料や不均一な試料でも解析できる。立体構造決定に至る前に、相互作用部位などの情報が得られる。とくに弱い相互作用のインタフェース決定に向いている。ミセルなどの不均一試料でも測定可能なので、膜結合蛋白質や膜蛋白質解析に向いている。小さい蛋白質ドメインに向いている。方法論を開発する余地が多く残っている。試料標識法の改良など遺伝子工学的にもアプローチする余地がある。In-cell NMR法みたいなヘンな測定法が開発可能。
悪い点:立体構造決定可能な分子の大きさに制限がある。大きいものには向かない。しかも決定された構造の分解能が低い。「分子置換法」に相当する方法がないので、既知構造のバリアント構造決定については、速度がとても遅い。試料に安定同位体を導入しないといけないので試料調製がめんどくさい。方法論が未熟なので、ルーチンワークにしにくく、勉強することがおおいので、めんどくさい。
以上のことを総合して、それでもNMR構造生物学にはこれからも面白い発見がたくさんあるでしょう。NMRのよい点に、ほかの方法論の優れた点を組み合わせて、やりがいのある研究をしていきませんか?